Les glandes parathyroïdes, composantes de l’anatomie du système endocrinien humain, jouent un rôle particulier dans le maintien de l’homéostasie calcique. Bien qu’elles soient souvent méconnues du grand public, leur importance pour la régulation métabolique est capitale.
Copyright AKIVI
Cette documentation anatomique a été rédigée par les rédacteurs de l’application AKIVI. Elle a été par la suite validée puis complétée par le Docteur Florian Bernard – neurochirurgien au CHU d’Angers et maître de conférences en anatomie à l’Université d’Angers. L’intégralité de ce document a été certifié par les professeurs d’anatomie français partenaires d’AKIVI.
Documentation actualisée le 24 février 2025
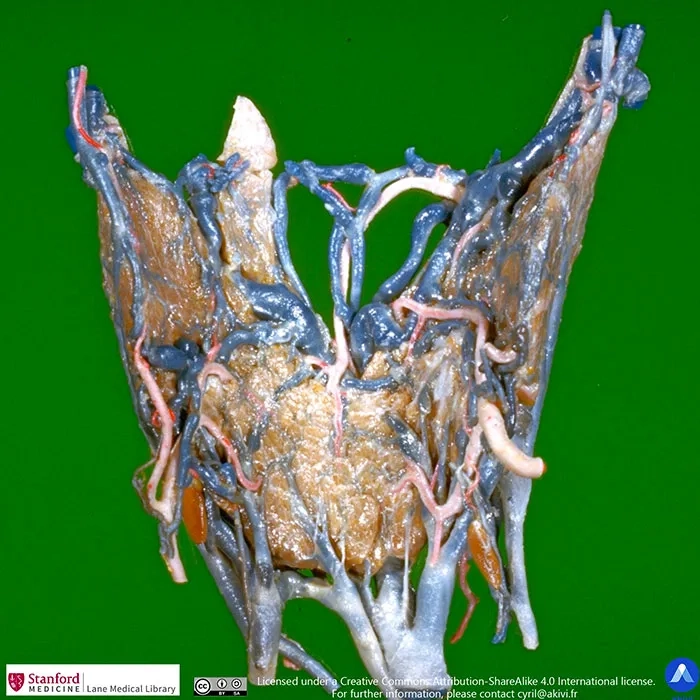
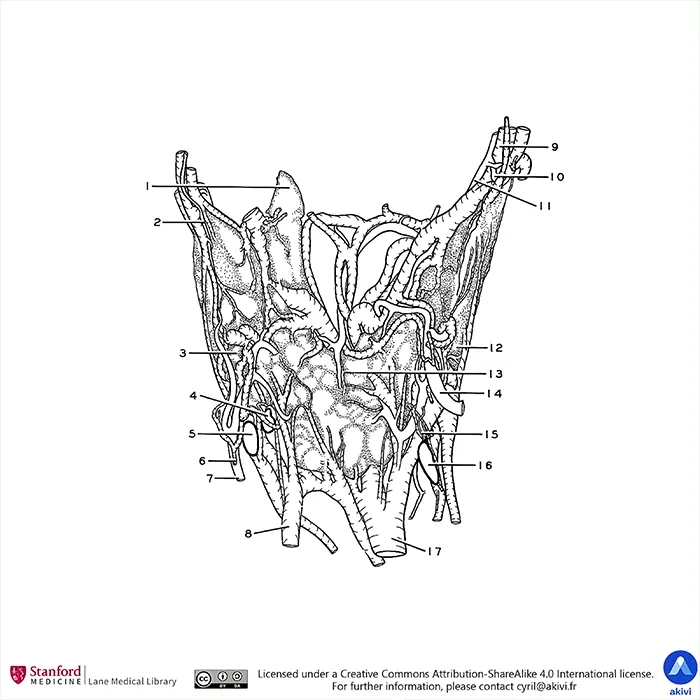
Légende du schéma complétant la coupe anatomique des glandes parathyroïdes : 1. Lobe pyramidal – 2. Branche postérieure de l’artère thyroïdienne supérieure – 3. Lobe gauche – 4. Glande parathyroïdienne supérieure gauche – 5. Glande parathyroïdienne inférieure gauche – 6. Veine thyroïdienne moyenne – 7. Artère thyroïdienne inférieure gauche – 8. Veine thyroïdienne inférieure gauche – 9. Veine thyroïdienne supérieure droite – 10. Branche postérieure de l’artère thyroïdienne supérieure – 11. Branche antérieure de l’artère thyroïdienne supérieure – 12. Lobe droit – 13. Isthme – 14. Artère thyroïdienne inférieure droite – 15. Artère vers la glande parathyroïdienne inférieure droite – 16. Glande parathyroïdienne inférieure droite – 17. Veine thyroïdienne inférieure droite
Le terme « parathyroïde » provient du grec ancien para, signifiant « près de », et « thyroïde », en référence à leur localisation adjacente à la glande thyroïde.
Définies comme des glandes endocrines, les glandes parathyroïdes sécrètent une hormone spécifique, la parathormone (PTH), indispensable au métabolisme du calcium et du phosphate.
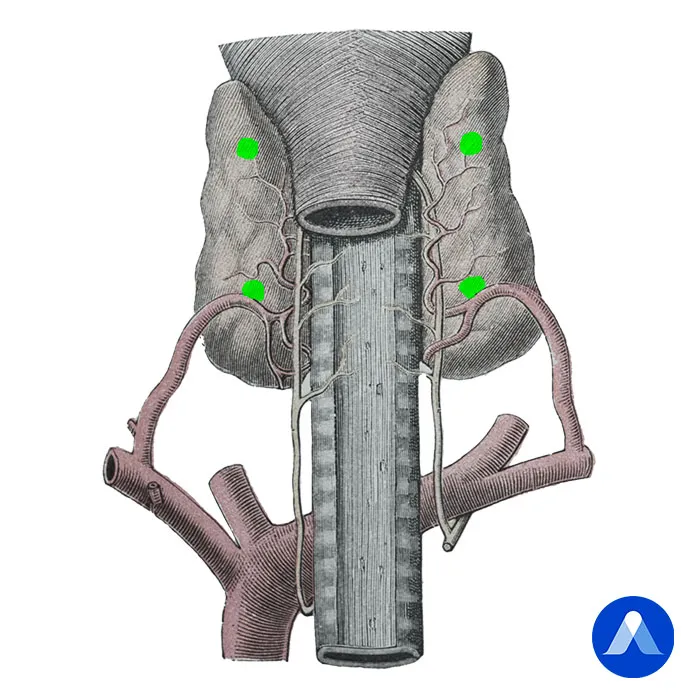
Les glandes parathyroïdes sont généralement au nombre de quatre, bien que des variations anatomiques soient fréquentes (trois à cinq glandes). Elles sont situées sur la face postérieure des lobes thyroïdiens, réparties en deux paires :
• Parathyroïdes supérieures : issues de la 4ᵉ poche pharyngée.
• Parathyroïdes inférieures : issues de la 3ᵉ poche pharyngée.
Chaque glande est enveloppée d’une fine capsule fibreuse et mesure environ 5 mm de diamètre pour un poids total de 25 à 50 mg.
• Rapports antérieurs : lobes thyroïdiens.
• Rapports postérieurs : fascia cervical profond.
• Rapports latéraux : gaine neurovasculaire cervicale (carotide commune, veine jugulaire interne, nerf vague).
• Rapports inférieurs : trachée et œsophage.
• Artères : Les glandes parathyroïdes sont vascularisées principalement par les artères thyroïdiennes inférieures, avec des contributions occasionnelles des artères thyroïdiennes supérieures.
• Veines : Drainage assuré par les veines thyroïdiennes qui se jettent dans les veines jugulaires internes ou brachiocéphaliques.
• Innervation : Principalement sympathique, dérivée des ganglions cervicaux, jouant un rôle limité dans la régulation hormonale.
Les glandes parathyroïdes sont composées de deux types cellulaires principaux :
• Cellules principales : responsables de la sécrétion de la parathormone (PTH), elles sont petites et disposées en cordons.
• Cellules oxyphiles : de fonction encore incertaine, elles apparaissent après la puberté et sont souvent plus volumineuses.
Un tissu conjonctif lâche entoure les cellules glandulaires, abritant un réseau dense de capillaires sanguins et lymphatiques facilitant une régulation hormonale rapide.
La PTH est la principale hormone sécrétée par les glandes parathyroïdes. Sa libération est régulée par le taux de calcium ionisé dans le plasma, via des récepteurs sensibles au calcium (CaSR) situés à la surface des cellules principales.
• Os : Stimule l’activité des ostéoclastes, augmentant la résorption osseuse et libérant du calcium et du phosphate dans le sang.
• Reins : Réduit l’excrétion rénale de calcium tout en augmentant celle du phosphate.
• Intestin : Favorise l’absorption intestinale du calcium en stimulant la production de calcitriol (forme active de la vitamine D).
La sécrétion de PTH est soumise à un mécanisme de rétrocontrôle négatif basé sur les concentrations plasmatiques de calcium. Une hypocalcémie stimule la sécrétion de PTH, tandis qu’une hypercalcémie l’inhibe.
Les glandes parathyroïdes dérivent des 3ᵉ et 4ᵉ poches pharyngées. Les parathyroïdes inférieures migrent avec le thymus pour atteindre leur position finale, tandis que les parathyroïdes supérieures descendent légèrement pour s’installer sur la partie postérieure de la thyroïde. Des anomalies de migration peuvent entraîner des parathyroïdes ectopiques.

• Hyperparathyroïdie primaire : due à un adénome parathyroïdien, une hyperplasie ou, plus rarement, un carcinome.
• Hyperparathyroïdie secondaire : conséquence de l’insuffisance rénale chronique entraînant une hypocalcémie persistante.
• Hyperparathyroïdie tertiaire : hyperfonction autonome des glandes parathyroïdes après une stimulation prolongée.
• Hypoparathyroïdie : souvent d’origine post-chirurgicale ou auto-immune, elle se traduit par une hypocalcémie sévère.
• Adénome parathyroïdien : tumeur bénigne responsable de la majorité des hyperparathyroïdies primaires.
• Carcinome parathyroïdien : rare, mais associé à une hypercalcémie sévère.
• Dosages hormonaux : PTH sérique, calcémie ionisée et totale, phosphatémie.
• Vitamine D : évaluation de la concentration de calcitriol.
• Échographie cervicale : localisation des glandes hypertrophiées.
• Scintigraphie au sestamibi : méthode sensible pour identifier les adénomes parathyroïdiens.
• IRM ou scanner cervical : utiles en cas de parathyroïdes ectopiques.
La biopsie permet de confirmer la nature bénigne ou maligne d’une tumeur.

Les glandes parathyroïdes furent découvertes pour la première fois en 1850 par Sir Richard Owen chez un rhinocéros indien. Leur découverte chez l’humain suivit peu après mais leur rôle physiologique resta longtemps inconnu. Au début du XXe siècle, des chercheurs commencèrent à établir le lien entre la PTH et l’homéostasie calcique. L’un des moments marquants fut la réalisation par Felix Mandl, en 1925, de la première parathyroïdectomie pour traiter une hyperparathyroïdie primaire. Cette intervention révolutionna la prise en charge des pathologies endocriniennes.
En parallèle, les premiers travaux expérimentaux sur les animaux révélèrent l’impact de l’ablation des glandes parathyroïdes, provoquant des crises de tétanie dues à une hypocalcémie sévère. Ces études renforcèrent la compréhension de leur rôle vital dans le métabolisme calcique.
Dans les années 1950, l’introduction de la scintigraphie permit une localisation plus précise des glandes parathyroïdiennes, particulièrement en cas de variations anatomiques. Cette avancée technologique facilita les interventions chirurgicales, réduisant les complications liées à leur ablation.
Une autre avancée majeure vint de l’identification des récepteurs sensibles au calcium (CaSR) dans les années 1990. Cette découverte ouvrit la voie à des traitements pharmacologiques ciblés pour les hyperparathyroïdies, notamment via des calcimimétiques.
Aujourd’hui, les glandes parathyroïdes continuent de susciter un intérêt croissant, avec des recherches focalisées sur les thérapies géniques pour corriger les dysfonctions congénitales et les anomalies héréditaires.

En France, l’Hôpital Européen Georges-Pompidou et l’Hôpital Cochin sont réputés pour leur expertise en pathologies parathyroïdiennes.
À l’international, la Mayo Clinic (États-Unis) et le Karolinska Institute (Suède) se distinguent par leurs innovations en chirurgie endocrinienne et en recherche sur les glandes parathyroïdes.
Tutoriel sur les cours d'anatomie de l'application AKIVI
Découvrez les 8 autres glandes et organe constituant le système endocrinien de l’homme et de la femme :
Le pancréas possède une organisation anatomique en trois parties : la tête, accolée au duodénum, le corps, en avant des gros vaisseaux abdominaux, et la queue, proche de la rate.

La thyroïde est constituée de follicules thyroïdiens, unités fonctionnelles contenant la thyroglobuline, précurseur des hormones thyroïdiennes.

La glande pinéale est richement vascularisée par les branches de l’artère cérébrale postérieure, assurant un apport sanguin adapté à son activité hormonale.

Une altération des fonctions de l’hypothyse peut entraîner des pathologies variées, telles que l’hypopituitarisme, l’acromégalie ou le syndrome de Cushing.

En réponse au stress, la médullosurrénale (glande surrénale) libère de l’adrénaline, accélérant le rythme cardiaque et augmentant la disponibilité du glucose dans le sang.

L’hypothalamus contrôle le cycle veille-sommeil via la sécrétion de neuropeptides comme les hypocretines (orexines).

Les testicules jouent un rôle central dans la fonction reproductrice et hormonale masculine, régulés par l’axe hypothalamo-hypophyso-gonadique via la GnRH, la LH et la FSH.

Les ovaires sont aussi impliqués dans la production d’androgènes en faible quantité, jouant un rôle dans la libido et le métabolisme féminin.
AKIVI propose des milliers de vidéos, images, QCM, dissections 3D et cas cliniques pour apprendre l’anatomie où que vous soyez.
Téléchargez notre application sur votre smartphone ! Une adresse mail et un mot de passe suffisent pour créer votre compte « Freemium » et ainsi utiliser gratuitement AKIVI sur mobile, tablette ou ordinateur.

AKIVI propose des milliers de vidéos, images, QCM, dissections 3D et cas cliniques pour apprendre l’anatomie où que vous soyez.
Téléchargez notre application sur votre smartphone ! Une adresse mail et un mot de passe suffisent pour créer votre compte « Freemium » et ainsi utiliser gratuitement AKIVI sur mobile, tablette ou ordinateur. »
